El objetivo de este trabajo fue el estudio de los parámetros cinéticos de la cristalización isotérmica de fases grasas a distintas temperaturas mediante calorimetría diferencial de barrido (DSC, por su sigla en inglés). Las fases grasas consistieron en mezclas de aceite de salvado de arroz completamente hidrogenado (FHRBO) y aceite de soja (SBO) en diferentes proporciones (20, 25, 30, 35 y 40 % de FHRBO), siendo ambos materiales previamente purificados. Además, se seleccionaron algunas de las mezclas y se les adicionó una cantidad conocida de fitoesteroles. Los parámetros cinéticos fueron obtenidos aplicando el modelo de Avrami, el cual determina el período de inducción (generación de núcleos cristalinos, ti), el mecanismo de nucleación (exponente de Avrami, n) y el grado de crecimiento cristalino (constante cinética de velocidad, k). Se observó que a mayor contenido de FHRBO y menor temperatura de cristalización, ti se reduce y k aumenta, llevando a una cinética más rápida, lo cual era esperable por el aporte de triglicéridos tri-saturados y un mayor grado de sobreenfriamiento. En la mezcla con 35 % de FHRBO, el agregado de fitoesteroles enlenteció la cinética (aumento de ti y reducción de k); sin embargo, en la de 20 % de FHRBO aumentó tanto ti como k.
Palabras clave: modelo de Avrami, sobreenfriamiento, composición lipídica, componentes menores.
O objetivo deste trabalho foi estudar os parâmetros cinéticos da cristalização isotérmica de misturas graxas em diferentes temperaturas por calorimetria diferencial de varredura (DSC). As misturas graxas consistiam em óleo de farelo de arroz totalmente hidrogenado (FHRBO) e óleo de soja (SBO) em diferentes proporções (20, 25, 30, 30, 35 e 40 % FHRBO), sendo ambos os materiais previamente purificados. Além disso, algumas das misturas foram selecionadas e uma quantidade conhecida de fitoesteróis foi adicionada a elas. Os parâmetros cinéticos foram quantificados pela aplicação do modelo de Avrami que determina o período de indução (geração de núcleos cristalinos, ti), o mecanismo de nucleação (expoente de Avrami, n) e o grau de crescimento do cristal (constante cinética, k). Observou-se que quanto maior e a proporçõe de FHRBO e menor a temperatura de cristalização ti diminui e k aumenta, levando a uma cinética mais rápida, o que é consistente com a contribuição de triglicerois tri-saturados e maior grau de super-resfriamento. Na mistura com 35 % de FHRBO, a adição de fitoesteróis promoveu um aumento de ti e redução de k, prolongando a nucleação e retardando o crescimento dos cristais. Por outro lado, na mistura com 20 % de FHRBO observou-se aumento de ti e k.
Palavras-chave: modelo do Avrami, super-resfriamento, composição lipídica, componentes menores.
Introducción
Las grasas y los aceites comestibles son básicamente mezclas complejas de triglicéridos (TAG), compuestos mayoritarios constituyentes de estos materiales en aproximadamente un 95 % (Marangoni, 2013a). Por este motivo, la composición en ácidos grasos y la manera en la que se distribuyen en los TAG son el factor determinante sobre sus propiedades de cristalización (Marangoni, 2013a). Cuando un material graso cristaliza, se lleva a cabo un proceso complejo que implica la formación de una red cristalina. Las características de esa red cristalina dependen del comportamiento de cristalización, el cual está influenciado por los tipos de TAG presentes, y por cómo interactúan y se empaquetan espacialmente (Basso et al., 2010).
Antes del comienzo de la cristalización de un TAG en el material graso, este último debe estar en una condición termodinámica favorable para promover la generación de un sólido a partir de una fase líquida (Toro-Vazquez et al., 2002). Esta condición es conocida como sobreenfriamiento, la cual ocurre a partir de temperaturas por debajo de la temperatura de cristalización del material graso sin que la cristalización se haya iniciado. En esa condición, los TAG forman pequeños agregados cristalinos no estables en equilibrio con la fase líquida (Marangoni, 2013b). Para que se promueva la obtención de agregados estables (núcleos cristalinos) se requiere tiempo, siendo por lo general un proceso lento. Una vez que se obtienen los agregados estables, el proceso de cristalización ocurre de forma espontánea (Marangoni, 2013b). Estos agregados continúan creciendo, formando así los cristales. Los cristales formados pueden generar interacciones entre ellos, conduciendo a la conformación de la red cristalina (Basso et al., 2010).
La cristalización cumple un rol muy importante en productos como el chocolate, las cremas para untar y las margarinas (Sato, 2001; Hubbes et al., 2018). Si bien las características de la red cristalina obtenida en este tipo de productos influyen en la textura y las propiedades viscoelásticas, estudiar la cinética de la cristalización permite conocer más en detalle los fenómenos anteriormente mencionados que ocurren durante el desarrollo de dicha red.
Por lo general, los materiales grasos que se destinan para su uso en alimentos suelen presentar características particulares. La más importante es que no presenten ácidos grasos trans de origen industrial, ya que diversos estudios nutricionales han demostrado la relación directa entre el consumo de estos ácidos grasos y el incremento en los niveles de lipoproteínas de baja densidad (LDL) y la disminución de lipoproteínas de alta densidad (HDL), provocando un aumento en el riesgo de padecer una enfermedad cardiovascular (Oteng y Kersten, 2020). La industria alimentaria ha tenido que recurrir a cambios en los materiales grasos para cumplir con este aspecto. En términos generales, alternativas tecnológicas como la hidrogenación completa, el mezclado y la interesterificación han mostrado ser convenientes y versátiles para el diseño de materiales grasos comestibles cero-trans (Ribeiro et al., 2009; Zuher et al., 2018; Segura y Jachmanián, 2020; Callejas et al., 2021).
Las mezclas suelen estar constituidas por materiales grasos en diferentes proporciones, generalmente un aceite y otro material que aporte un contenido de ácidos grasos saturados, de modo tal que les confiera estructura y consistencia. De esta forma la mezcla resultante presenta el suficiente contenido de sólidos para dar estabilidad a la red cristalina formada. Dentro de los aceites se destaca el aceite de soja (SBO) por ser económico, por estar disponible en grandes cantidades, por sus cualidades nutricionales (alto aporte de ácidos grasos linoleico y linolénico) y por su alta funcionalidad, lo que lo convierte en una materia prima interesante (Ribeiro et al., 2009).
Dentro de los materiales grasos con alto grado de saturación, el aceite de palma, la grasa vacuna y los aceites vegetales completamente hidrogenados han funcionado exitosamente como materia prima (Zuher et al., 2018; Segura y Jachmanián, 2020; Callejas et al., 2021). Estos últimos, a diferencia de los aceites parcialmente hidrogenados, no contienen ácidos grasos trans.
La cinética de la cristalización es característica de cada material graso y depende de las propiedades fisicoquímicas del material y del tratamiento de enfriamiento aplicado (Mursalin et al., 2016). Mediante el análisis de la cinética de cristalización es posible obtener parámetros cinéticos importantes tales como el mecanismo de nucleación y la velocidad de crecimiento cristalino (Mursalin et al., 2016).
El proceso de cristalización en materiales grasos puede ser estudiado a través de diferentes modelos (Toro-Vazquez et al., 2002). Sin embargo, el que se utiliza más frecuentemente es el modelo de Avrami (Narine et al., 2006). El modelo de Avrami fue desarrollado originalmente para describir la cinética de transición de líquido a sólido en metales (Avrami, 1941). Luego se aplicó a la cristalización de polímeros (Sharples, 1966); mientras que en lípidos, los primeros estudios se realizaron para describir la nucleación y cristalización del aceite de palma (Kawamura, 1980).
La expresión básica en condiciones isotérmicas de la ecuación del modelo de Avrami está dada por:
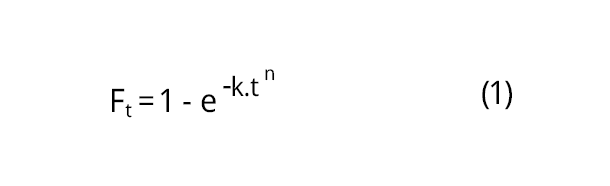
Donde Ft es la cristalización relativa y representa la fracción de una variable vinculada al estado sólido de la muestra, definida generalmente como la relación entre la variable a tiempo “t” y su valor máximo a la temperatura de cristalización. La constante k representa la velocidad de crecimiento cristalino y es función de la temperatura. El exponente de Avrami (n), también referido como índice de cristalización, indica el mecanismo de crecimiento cristalino. Dicho parámetro es una función combinada que depende del tiempo, el tipo de nucleación (esporádica o instantánea) y el número de dimensiones en el cual tiene lugar el crecimiento cristalino (Hubbes et al., 2018).
Los parámetros cinéticos del modelo se obtienen por medio de datos experimentales a lo largo del tiempo. Según Mursalin et al. (2016), los datos experimentales que se utilizan para ajustar el modelo son obtenidos por medio del contenido de sólidos (SFC), determinado por resonancia magnética nuclear de pulsos (p-RMN); o por la entalpía de cristalización, determinada por calorimetría diferencial de barrido (DSC). La técnica más adecuada para caracterizar el proceso de cristalización es p-RMN (Foubert et al., 2003). Sin embargo, la técnica de DSC presenta como ventajas un estricto control de temperatura y un pequeño tamaño de muestra que reduce la influencia de agentes externos en la cristalización (Foubert et al., 2003). Por lo mencionado anteriormente, la técnica de DSC, muy utilizada en el área de los lípidos, es capaz de proporcionar datos cinéticos confiables y reproducibles a partir de los termogramas de cristalización isotérmica (MacNaughtan et al., 2006). Sumado a lo anterior, permite determinar propiedades asociadas con la fusión del material graso (Supaphol y Spruiell, 2000).
Si bien la presencia de compuestos minoritarios (fosfolípidos, glicéridos parciales y compuestos con carácter antioxidante) en los materiales grasos es baja, presentan una mayor polaridad y en algunos casos un comportamiento anfifílico con respecto a los triglicéridos. Estos compuestos han sido considerados agentes que afectan la cristalización (Metin y Hartel, 2005; Smith et al., 2011; Buscato et al., 2018).
Los fitoesteroles muestran un gran interés comercial debido a las implicancias positivas en la salud humana (reducción del LDL) y se encuentran presentes, en contenidos muy bajos, en los aceites vegetales, granos y frutos (Daels et al., 2018). Katan et al. (2003) reportó que los fitoesteroles son responsables de la disminución de aproximadamente un 10 % del LDL en la sangre humana. Debido a eso, resulta atractiva la adición de esta clase de compuestos en los materiales grasos como ingrediente para formulaciones de alimentos funcionales. En la industria alimentaria, los fitoesteroles se agregan en formulaciones de margarinas (Belitz et al., 2009). Sin embargo, su adición podría influenciar el comportamiento de la cristalización y generar problemas durante el proceso de producción o en las propiedades mecánicas (Daels et al., 2017).
En este estudio, las mezclas preparadas fueron enfriadas rápidamente hasta alcanzar diferentes temperaturas de cristalización a los efectos de promover su cristalización isotérmica. El objetivo fue determinar el efecto de la temperatura de cristalización, la composición química de las mezclas y el agregado de diferentes contenidos de fitoesteroles sobre la cinética de cristalización. La ecuación del modelo de Avrami fue utilizado para obtener los parámetros cinéticos asociados al mecanismo de nucleación y al crecimiento cristalino.
Materiales y Métodos
Se utilizaron dos materiales grasos: aceite de soja refinado (SBO), marca Río de la Plata (Uruguay), el cual fue adquirido en un comercio local; y aceite de salvado de arroz completamente hidrogenado (FHRBO), obtenido previamente mediante un proceso de hidrogenación completa en un reactor Parr de 250 mL (4570HP/HT Parr Instrument Company, Illinois, USA), montado y puesto a punto en el Área Grasas y Aceites del Departamento de Ciencia y Tecnología de los Alimentos de la Facultad de Química (Udelar), para dicho fin (Callejas et al., 2021). La hidrogenación fue realizada bajo 15 bar de presión de H2 y 120 ℃, utilizando un 5 % en peso de un catalizador comercial (PRICAT 9910, de Johnson Matthey, London, UK). Luego de 3 horas de reacción el FHRBO fue obtenido, verificándose que la reacción fuera completa por análisis de la composición en ácidos grasos (método descrito más adelante), que muestra la ausencia de ácidos grasos trans en el material graso. Los fitoesteroles consistieron en una mezcla de Brassicasterol (11 %), Campesterol (39 %) y β-sitoesterol (51 %), provistos por Sigma-Aldrich.
Previo a la obtención de las mezclas, ambos materiales grasos fueron purificados con el propósito de remover el contenido de compuestos minoritarios como tocoferoles, fitoesteroles, ácidos grasos libres, monoglicéridos y diglicéridos. Para esto, se hizo fluir por gravedad cada material graso por una columna con alúmina neutra activada según el método AOCS (American Oil Chemist´s Society, 2009a). Como resultado de la purificación se verificó la remoción de un 99 % de tocoles totales (tocoferoles + tocotrienoles). Este análisis indirecto permitió inferir que la columna con alúmina fue capaz de remover en gran medida otros compuestos con grupos químicos de similares características a las de los tocoferoles (como los fitoesteroles y glicéridos parciales).
Preparación de las mezclas
Cinco mezclas con contenidos de FHRBO desde 20 hasta 40 %, en incrementos del 5 % en peso, fueron preparadas mezclando cada material graso en viales de 4 mL hasta alcanzar una masa final próxima a los 2 gramos de mezcla. Luego fueron venteadas con nitrógeno y cerradas herméticamente para ser transferidas a un agitador orbital a 200 rpm durante 15 minutos a 70 ℃ para su completa homogenización.
Mezclas con agregado de fitoesteroles
A las mezclas con 20 y 35 % de FHRBO se les agregaron diferentes contenidos de fitoesteroles (1 %, 2 % y 4 % en peso). Para esto se prepararon 8 gramos de mezcla, luego se separaron 2 gramos a los cuales se les adicionó el contenido de fitoesteroles correspondiente, obteniéndose tres sistemas compuestos por una mezcla de composición definida con diferentes niveles de fitoesteroles. Luego todas las mezclas con fitoesteroles fueron venteadas con nitrógeno y cerradas herméticamente para ser transferidas a un agitador orbital a 200 rpm durante 15 minutos a 70 ℃ hasta su completa solubilización y homogenización.
Determinación de la composición en ácidos grasos
Los materiales grasos (SBO y FHRBO) fueron previamente derivatizados a sus correspondientes ésteres metílicos según AOCS (American Oil Chemist´s Society, 2009b). Los ésteres fueron luego analizados por GC utilizando un cromatógrafo Shimadzu modelo 14B equipado con FID y una columna capilar Supelco SP2330 (30 m x 0,25 mm x 0,20 μm). El programa de temperatura inició a los 160 ℃, se aumentó la temperatura hasta los 225 ℃ a una velocidad de 5 ℃/min, y luego se mantuvo a dicha temperatura durante 10 minutos. Se utilizó nitrógeno como gas portador. La identificación de los ácidos grasos se llevó a cabo por comparación de los tiempos de retención con los correspondientes al análisis de un estándar de ésteres metílicos de los ácidos grasos (provistos por Sigma-Aldrich), bajo las mismas condiciones cromatográficas. Los análisis fueron realizados por duplicado y el promedio de los valores, informado.
Determinación de la composición en triglicéridos
Los materiales grasos (SBO y FHRBO) fueron disueltos en acetona (30 mg/mL), y la separación de los triglicéridos y su composición fueron analizadas directamente por cromatografía líquida de alta resolución (HPLC) en un cromatógrafo Shimadzu Prominence modelo 20A según AOCS (American Oil Chemist´s Society, 2009c), con algunas modificaciones. El sistema se equipó con un detector de índice de refracción (RID) Shimadzu modelo 10A y dos columnas Supelcosil TM C18 (25 cm x 4.6 mm x 5 um), y se inyectaron 40 μL de muestra. El análisis partió de una mezcla inicial de acetona/acetonitrilo/cloroformo 47, 5:47, 5:5, que se mantuvo constante durante todo el tiempo de análisis (45 minutos) a un flujo de 1 mL/min. La identificación se llevó a cabo utilizando estándares puros de TAG y materiales grasos de composición conocida considerando el orden de elución de acuerdo con el número equivalente de carbono (ECN). Los análisis fueron realizados por duplicado y el promedio de los valores, informado.
Obtención de los termogramas de fusión
Los termogramas de fusión se determinaron mediante calorimetría diferencial de barrido (DSC) en un calorímetro marca Shimadzu modelo 60A plus, equipado con un sistema de refrigeración Thermo scientific EK90/SH según AOCS (American Oil Chemist´s Society, 2009d). Para esto se colocaron entre 10-15 mg de muestra dentro de una cápsula de aluminio, la cual fue calentada hasta los 90 ℃ para asegurar la fusión completa, seguido de un enfriamiento a 10 ℃/min hasta -50 ℃. Luego se mantuvo a esa temperatura por 30 minutos y finalmente se llevó a cabo una etapa de calentamiento a 5 ℃/min hasta la fusión completa. En esta última etapa se registró el flujo de calor endotérmico de la muestra, obteniéndose así el termograma de fusión correspondiente. El procesamiento de los datos se realizó utilizando el software correspondiente (Shimadzu Corporation, 2009). Para la calibración del equipo se utilizó un patrón de Indio de alta pureza suministrado por Sigma-Aldrich. Los análisis fueron realizados por duplicado.
Obtención de las isotermas de cristalización
Usando la misma cápsula con la muestra con la que se obtuvo el termograma de fusión fue posible realizar un seguimiento de la cristalización isotérmica. Para esto, previo a su enfriamiento, la muestra fue sometida a una etapa de calentamiento a 90 ℃, que se mantuvo durante 10 minutos, para remover los cristales que pudiera tener presente con el fin de borrar la memoria cristalina del material graso. Luego se la enfrió rápidamente (a la máxima potencia que puede suministrar el sistema de refrigeración) hasta alcanzar la temperatura de cristalización (35, 38, 40 y 42 ℃). Una vez alcanzada dicha temperatura, se mantuvo constante hasta finalizar el proceso de cristalización. En esta etapa se registró el flujo de calor exotérmico de la muestra obteniéndose la isoterma de cristalización correspondiente a cada muestra. El procesamiento de los datos se realizó utilizando el software correspondiente (Shimadzu Corporation, 2009). Los análisis fueron realizados por duplicado.
Análisis estadístico
Algunos datos fueron sujetos a un análisis de varianza (ANOVA) utilizando el software correspondiente (Di Rienzo et al., 2020). Diferencias significativas entre los valores medios fueron comparadas utilizando el test de Tukey con un nivel de confianza del 95 % (p < 0,05).
Resultados y Discusión
Composición en ácidos grasos y triglicéridos
En la Tabla 1 se muestra la composición en ácidos grasos de los materiales grasos de partida (FHRBO y SBO) y de las mezclas preparadas con diferentes contenidos de FHRBO. En el SBO, el ácido graso presente en mayor proporción fue el linoleico, seguido del oleico y el palmítico. Dicha composición concuerda con resultados reportados por otros autores en diferentes estudios (Ali et al., 2019; Ribeiro et al., 2009). En relación con el FHRBO, los principales ácidos grasos fueron el palmítico y el esteárico. Dicha composición es reflejo de la composición inicial del aceite de salvado de arroz (RBO) y la conversión de todos los ácidos grasos insaturados de 18 átomos de carbono presentes a su ácido graso saturado correspondiente durante el proceso de hidrogenación completa (Callejas et al., 2021). Es de destacar la ausencia de ácidos grasos trans en este tipo de materiales, lo que confirma la efectividad del proceso de hidrogenación completa.
Tabla 1. Composición en ácidos grasos (% m/m) de los materiales grasos de partida (FHRBO y SBO) y sus respectivas mezclas con diferentes contenidos de FHRBO.

nd: no detectado
En relación con las mezclas FHRBO/SBO, la incorporación de FHRBO llevó a cambios inherentes en la composición en ácidos grasos, los cuales ocurrieron progresivamente en función del porcentaje de FHRBO agregado. Se observó que al incrementar el porcentaje de FHRBO desde 20 a 40 %, el contenido en ácidos grasos insaturados y poliinsaturados (18:1, 18:2 y 18:3) disminuyó; en contraposición, los niveles de SFA aumentaron.
La Tabla 2 muestra la composición en TAG individuales del FHRBO, SBO y de las mezclas preparadas con diferentes contenidos de FHRBO, así como también los diferentes grupos de TAG asociados según los tipos de ácidos grasos saturados o insaturados que los constituyen. De esta forma, se obtuvieron 4 tipos de TAG (tri-saturados, S3; di-saturados, S2U; di-insaturados, U2S y tri-insaturados, U3). Los TAG LLL, OLL y PLL fueron mayoritarios en el SBO, lo cual coincide con lo reportado por otros autores (Gunstone y Harwood, 2007; Ribeiro et al., 2009). En el FHRBO fueron identificados únicamente los TAG tri-saturados, siendo StStSt el mayoritario, seguido de PStSt y PStP. LLL y OLL fueron los TAG mayoritarios en las mezclas con 20 y 25 % en FHRBO, mientras que LLL y StStSt lo fueron en la mezcla con 30 % en FHRBO. En cambio, los TAG StStSt y PStSt fueron los predominantes en las mezclas con 35 y 40 % en FHRBO.
La sumatoria de TAG del tipo S3 y U3 (mayoritarios en ambos materiales grasos) constituyó más del 70 % en todas las mezclas, predominando los TAG del tipo U3, a excepción de la mezcla con 40 % en FHRBO.
Tabla 2. Composición en triglicéridos (% m/m) de los materiales grasos de partida (FHRBO y SBO) y sus respectivas mezclas con diferentes contenidos de FHRBO.

P: ácido palmítico, St: ácido esteárico, O: ácido oleico, L: ácido linoleico, Ln: ácido linolénico.
nd: no detectado.
Propiedades térmicas y comportamiento de fusión
Se obtuvieron los termogramas de fusión (gráfico de potencia vs temperatura o tiempo), en los cuales apartamientos positivos o negativos de la señal de potencia de la línea de base (cero) se vinculan a procesos exotérmicos (cristalización) o endotérmicos (fusión) ocurridos en el material graso. La Figura 1 muestra los termogramas de fusión obtenidos de las mezclas FHRBO/SBO preparadas con diferentes contenidos de FHRBO. La Tabla 3 presenta algunos parámetros de interés obtenidos a partir de los termogramas.
Los termogramas de fusión de las mezclas presentaron dos regiones endotérmicas bien definidas con temperaturas de pico relacionadas a la fusión de la fracción de TAG de bajo y alto punto de fusión (Tpf). Una región correspondiente a los TAG característicos del SBO con Tpf1 aproximadamente en -25 ℃, de baja temperatura de fusión, representados fundamentalmente por TAG del tipo U3, y la otra correspondiente a los TAG característicos del FHRBO con Tpf2 entre 58 y 62 ℃ aproximadamente, de alta temperatura de fusión, representados por TAG del tipo S3.
La temperatura de inicio de la fusión (Tif) no mostró una variación importante al aumentar el contenido de FHRBO en las mezclas. Otro efecto observado fue la disminución y el incremento de las entalpías de fusión ∆H1 y ∆H2, respectivamente, a medida que aumentó el agregado de FHRBO a las mezclas. Es posible afirmar que las mezclas combinaron propiedades térmicas de ambos materiales grasos, pareciéndose más a aquel que contienen en mayor proporción.
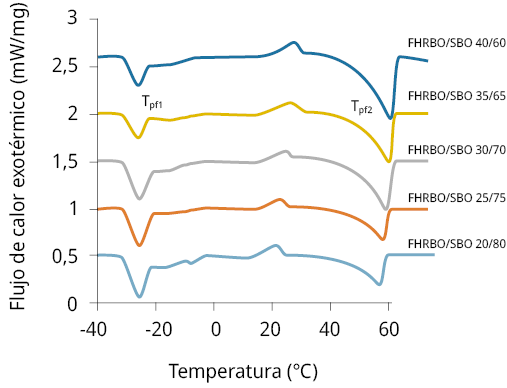
Figura 1. Termogramas de fusión de las mezclas FHRBO/SBO con diferente contenido de FHRBO. Tpfi: temperatura de fusión de pico 1 y 2 correspondientes a baja y alta temperatura, respectivamente.
La temperatura de fusión completa (Tfc) mostró una tendencia a incrementarse cuando aumentó el contenido de FHRBO. Si bien lo mencionado resultó esperable, un aspecto a considerar es que la variación de la Tfc al pasar del 20 % al 40 % en FHRBO aumentó solo 4,4 ℃. Estos resultados obtenidos coinciden con otros trabajos basados en mezclas con un aceite completamente hidrogenado (Ribeiro et al., 2009; Callejas et al., 2021; Ornla-ied et al., 2021).
Tabla 3. Parámetros obtenidos de los termogramas de fusión de las mezclas FHRBO/SBO con diferente contenido de FHRBO: temperatura de inicio de pico (Tif), temperatura de pico (Tpfi), entalpía de fusión del pico (ΔHi) y temperatura de fusión completa (Tfc).
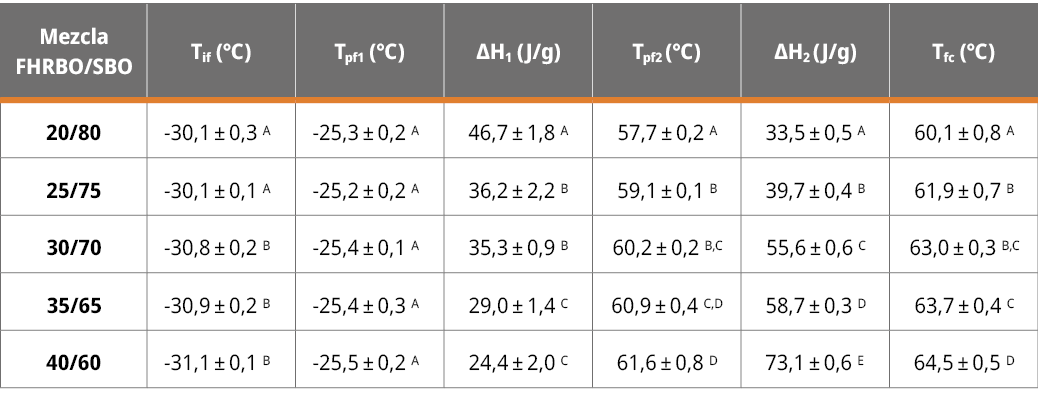
*Letras diferentes en la misma columna indican diferencias significativas entre las mezclas a un p < 0,05.
Estos resultados estarían indicando que la interacción entre ambos materiales grasos de la mezcla es muy pobre, confiriéndole a la mezcla las características propias de cada uno, atenuadas por su dilución frente al otro componente.
En todas las mezclas se observó un pequeño pico exotérmico (entre los 20 y 30 ℃ aproximadamente), que indica una transición polimórfica de alguna fracción de los sólidos del sistema. Este tipo de comportamiento también fue observado en mezclas de FHRBO con aceite de salvado de arroz (Callejas et al., 2021).
Cinética de la cristalización
La Figura 2 muestra un termograma típico de cristalización isotérmica para la mezcla FHRBO/SBO 30/70 a una temperatura de cristalización (Tc) de 42 ℃. Durante la cristalización de los materiales grasos bajo condiciones isotérmicas se asume que el flujo de calor exotérmico es directamente proporcional a la masa de la muestra y a la entalpía de cristalización (∆Hc) (Supaphol y Spruiell, 2000). Es posible obtener un parámetro denominado cristalización relativa (F) que representa la fracción del material graso al estado sólido a lo largo del tiempo, el cual puede ser obtenido por integración parcial a partir del termograma mostrado en la Figura 2. Para esto, se supone que la cristalización a una determinada temperatura finaliza cuando no se observa un cambio significativo en el valor de ∆Hc a un determinado tiempo luego de que la muestra cristaliza por completo (Supaphol y Spruiell, 2000).
F en función del tiempo se puede obtener según la siguiente expresión:

Donde ∆Hc,t. y ∆Hc,total representan el área entre el pico exotérmico y la línea de base desde el punto inicial hasta el tiempo t y el área total, respectivamente (Lu et al., 2021).

Figura 2. Termograma típico de la cristalización isotérmica de la mezcla FHRBO/SBO 30/70 y su correspondiente curva de cristalización relativa (F).
Para el análisis cinético del modelo de Avrami, los datos obtenidos de la cristalización relativa (F) se ajustan de acuerdo con la ecuación de Avrami (Ecuación 1) a través de su linealización según la siguiente expresión:
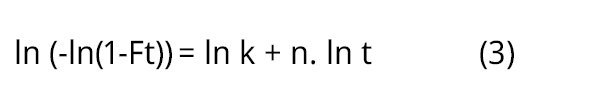
De esta manera, al graficar ln (-ln(1-Ft)) contra ln t es posible obtener de la pendiente el exponente de Avrami (n) y de la ordenada en el origen la constante de Avrami (k). Ambos representan los parámetros cinéticos de mayor interés.
Efecto de la composición de las mezclas y la temperatura de cristalización sobre los parámetros cinéticos: la Tabla 4 resume todos los parámetros cinéticos (ti, n y k) y el sobreenfriamiento (∆TS) de las mezclas FHRBO/SBO con diferente contenido de FHRBO a diferentes temperaturas de cristalización (Tc).
Tabla 4. Valores del período de inducción (ti), los parámetros k y n obtenidos mediante el modelo de Avrami y el sobreenfriamiento (ΔTS) de las mezclas FHRBO/SBO con diferente contenido de FHRBO a diferentes temperaturas de cristalización (Tc).

*En caso de cinética múltiple (n1, k1 y n2, k2) es posible determinar, por razones prácticas, una constante de velocidad global del proceso (k), que se calcula como la suma de las constantes involucradas (Hubbes et al., 2018). Letras diferentes en la misma columna indican diferencias significativas entre las mezclas a un p < 0,05.
El período de inducción (ti) en condiciones isotérmicas es definido como el tiempo necesario para la aparición de núcleos cristalinos a partir de los cuales se desencadena la cristalización (Himawan et al., 2006). Su determinación depende del tipo de método utilizado (Metin y Hartel, 2005), definiéndose en este caso como el tiempo para el cual F alcanza un valor de 0,01. Tal como puede observarse en la Tabla 4 e independiente del Tc estudiado, los valores de ti disminuyeron conforme aumentó el contenido de FHRBO en la mezcla, dado que aporta TAG del tipo S3, lo que favorece la aparición temprana de núcleos cristalinos. Además, las mezclas requieren de un grado de sobreenfriamiento para favorecer la cristalización. El sobreenfriamiento (ΔTS) se puede estimar como la diferencia entre la temperatura de fusión completa de las mezclas (Tfc, determinado a partir de los termogramas de fusión) y la Tc. El contenido de FHRBO de las mezclas tuvo influencia sobre la Tfc; por lo tanto, para una misma Tc, un menor contenido de FHRBO en las mezclas llevó a un sobreenfriamiento menor. Lo anterior es coherente y reafirma la relación inversa entre el ti y el contenido de FHRBO.
Al analizar una mezcla de composición fija de FHRBO a diferentes Tc, se observó que a mayor sobreenfriamiento, ti disminuye. El sobreenfriamiento juega un rol fundamental ya que es la fuerza motora de la cristalización. Un alto grado de sobreenfriamiento lleva a una disminución de la energía libre de activación para la formación de cristales estables, resultando en una rápida nucleación (Hubbes et al., 2018). Lo anterior explica por qué en la Tabla 4 existen mezclas a determinadas Tc en las cuales no se pudo analizar su cinética. La cristalización requiere de un adecuado grado de sobreenfriamiento y composición en TAG para verse favorecido. En condiciones de bajo sobreenfriamiento (Tc = 42 ℃), la cristalización no se ve favorecida salvo que la mezcla se enriquezca en TAG de alto punto de fusión. Es por esto que la mezcla con 20 % de FHRBO no mostró un pico exotérmico a lo largo de un tiempo muy prolongado (se dejó la muestra en el DSC durante más de 2 horas, pasado dicho tiempo se decidió finalizar el análisis).
Para la mezcla con 40 % de FHRBO y a una Tc = 38 ℃, ambas condiciones favorecieron la cristalización de forma tan rápida que la presencia del pico exotérmico se desarrolló mucho antes de alcanzar condiciones isotérmicas. Esto explica por qué para una Tc = 35 ℃ solo la mezcla con 20 % de FHRBO mostró una cristalización isotérmica.
Para obtener los parámetros cinéticos por medio de la linealización, según la Ecuación 3, se debe tener presente que no se aplica en todos los datos experimentales de la curva de F. En este caso, el criterio que se consideró fue tomar la mayor cantidad de valores posibles, de modo tal que el coeficiente de correlación (r2) sea superior a 0,98 en todos los casos (Narine et al., 2006; Hubbes et al., 2018). Se tomó inicialmente una región de F entre 0,25 y 0,75 (Toro-Vazquez et al., 2002), la cual se fue incrementando proporcionalmente entre los extremos y calculando el r2. Cuando el r2 cayó por debajo de 0,98; la región se consideró finalizada.
Con respecto a los valores de k, se observó que disminuyeron gradualmente al disminuir el porcentaje de FHRBO en las mezclas, lo que indica una velocidad de cristalización más lenta. Esto está relacionado con la disminución de los TAG del tipo S3, que se caracterizan por presentar una cristalización prácticamente instantánea (Marangoni, 2005). También, y al igual que lo observado para el ti, el ∆TS fue determinante sobre la velocidad. Se observó que el incremento del ∆TS llevó a un aumento de la constante de velocidad. Según Marangoni de Oliveira et al. (2015), el agregado de materiales con alto grado de saturación (llamados hard fats) en niveles de 1 al 5 % mostró cambios drásticos en el proceso de cristalización, con menores ti y mayores k a medida que se incrementó su contenido. En particular, determinaron que la tripalmitina (PPP) promovió el crecimiento del cristal, permitiendo una mayor acumulación y desarrollo de cristales. Si bien las mezclas preparadas no contenían PPP, sí presentaron un contenido considerable de StStSt de similares características, diferenciado únicamente en la longitud de cadena del ácido graso que lo conforma. Por lo que es muy probable que StStSt sea el TAG que promovió mayormente la alta velocidad de crecimiento cristalino en las mezclas, y por esta razón se incrementó considerablemente la k.
El exponente de Avrami “n” define la forma en que ocurre la nucleación y el crecimiento cristalino. Por lo tanto, cambios en dicho parámetro sugieren cambios en el modo de crecimiento de los cristales. Según Lu et al. (2021), un valor de n = 4 o inferior indica una nucleación heterogénea y crecimiento tipo esferulitas (esférico) a partir de un núcleo esporádico, donde el número de núcleos se incrementa linealmente con el tiempo. De forma similar, un valor de n = 3 indica crecimiento tipo esferulitas, pero a partir de un núcleo instantáneo. Un n = 2 indica crecimiento tipo platos o discos mayormente a lo largo de dos dimensiones, y un n = 1 representa crecimiento tipo agujas a partir de núcleos instantáneos. En la Tabla 4 se observó que, al igual que ocurre con el ti y la k, n se modifica en función de la composición de las mezclas y Tc. Un aumento en el contenido de FHRBO llevó a una disminución en el valor de n, pasando de una cristalización con crecimiento tipo esferulitas a uno mayormente del tipo platos. En ninguno de los casos se obtuvieron valores de n enteros. El principal motivo está asociado a que el crecimiento de cristales de diferentes características morfológicas puede ocurrir de manera simultánea debido a una cristalización heterogénea o a que cristales de similar morfología se desarrollan bajo un diferente tipo de nucleación (esporádica o instantánea). Distintos estudios realizados con mezclas de distintos materiales grasos (incluidos aceites completamente hidrogenados) han mostrado comportamientos similares en relación con el valor de n (Ribeiro et al., 2009; Lu et al., 2021).
Como se observa en la Tabla 4, algunas mezclas a determinadas Tc presentaron dos valores de n (n1 y n2) y dos valores de k (k1 y k2) debido a que los termogramas de cristalización mostraron la presencia de dos picos exotérmicos, obteniéndose curvas de F como la Figura 3.
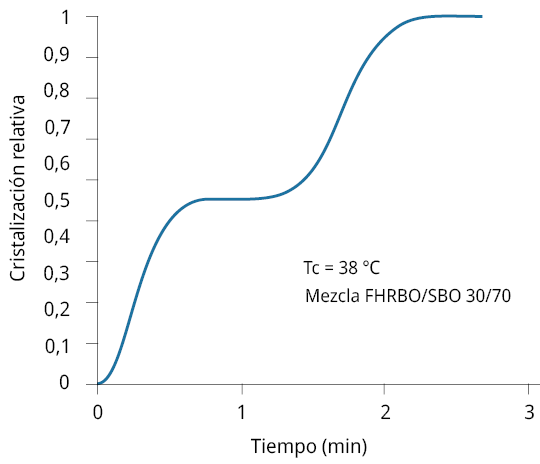
Figura 3. Curva de cristalización relativa (F) obtenida a partir de un termograma de cristalización con dos picos exotérmicos de la mezcla FHRBO/SBO 30/70.
Esto sugiere la co-cristalización de los TAG que conforman la mezcla, especialmente TAG del tipo S3 en combinación con los S2U. También puede estar indicando transformaciones polimórficas (Marangoni, 2013b). En los materiales grasos existe un fenómeno conocido como polimorfismo, que involucra la existencia de diferentes estructuras cristalinas (formas α, β´ y β, en orden creciente de estabilidad) con la misma composición química (Sato, 2001). Durante el proceso de cristalización, la forma polimórfica menos estable (α) será la más favorecida cinéticamente (de menor barrera energética para su formación y por lo tanto la menos limitada estructuralmente). Con el tiempo, las moléculas podrán reorganizarse dando lugar a formas termodinámicamente más estables (β´ y β), de menor estado energético (Marangoni, 2013c). Lo anterior constituye una “transformación polimórfica”, siendo procesos exotérmicos que tienen lugar hasta que se obtiene la estructura más estable (Marangoni, 2013c).
Este tipo de comportamiento se hace más evidente cuando las mezclas son ricas en FHRBO y se incrementa el ΔTS. Cuando el ΔTS es pequeño, el agregado de TAG al núcleo cristalino ocurre de manera lenta (bajos valores de k). Por lo tanto, los TAG tienen un tiempo suficiente para que el empaquetamiento se desarrolle bajo la configuración más apropiada y es de esperar que el polimorfo que se forme sea el más estable (cristalización bajo un único pico exotérmico).
A altos ΔTS ocurre todo lo contrario. La incorporación de TAG al núcleo cristalino es demasiado rápida, lo que provoca un empaquetamiento poco eficiente debido a la formación de diferentes cristales (cristales mixtos) y la coexistencia de distintos tipos de polimorfos (cristalización bajo dos o más picos exotérmicos). Cinéticas de cristalización de este tipo se han visto en materiales como la grasa láctea cristalizada a 10 ℃ (Marangoni, 2013b).
Efecto del agregado de fitoesteroles en las mezclas sobre los parámetros cinéticos: la Tabla 5 muestra los mismos parámetros cinéticos que la Tabla 4 para algunas mezclas de interés (FHRBO/SBO 35/65 y 20/80), con diferentes contenidos de fitoesteroles adicionados (1, 2 y 4 %) a dos Tc (38 y 40 ℃). En el caso de la mezcla con 35 % de FHRBO, se observó que el incremento de la concentración de fitoesteroles aumentó el ti y redujo la k a ambas Tc. Esto indica que la presencia de fitoesteroles genera una cinética de cristalización más lenta. Los componentes menores pueden afectar la nucleación, el crecimiento cristalino o ambos aspectos (Smith et al., 2011). El incremento del tiempo para la generación de núcleos cristalinos en este tipo de materiales grasos depende mayormente de la nucleación heterogénea. La presencia de un componente como los fitoesteroles, estructuralmente diferentes a los TAG, puede actuar como “blindaje” de los núcleos heterogéneos presentes, haciendo que estos sean menos eficientes como iniciadores de la cristalización (Smith et al., 2011).
Tabla 5. Valores del período de inducción (ti), los parámetros k y n obtenidos mediante el modelo de Avrami y el sobreenfriamiento (ΔTS) de dos mezclas FHRBO/SBO con diferente contenido de FHRBO y contenido de fitoesteroles (x % F) a dos temperaturas de cristalización (Tc).

*En caso de cinética múltiple (n1, k1 y n2, k2) es posible determinar, por razones prácticas, una constante de velocidad global del proceso (k), que se calcula como la suma de las constantes involucradas (Hubbes et al., 2018). Letras diferentes en la misma columna indican diferencias significativas entre las mezclas a un p < 0,05.
El efecto mencionado se hace más notorio a altas concentraciones de fitoesteroles. En términos generales, el agregado de 1 y 2 % no modificó prácticamente el ti; sin embargo, con un 4 % sí se observó un aumento. También explicaría por qué la cinética de crecimiento cristalino es más lenta, ya que al estar los fitoesteroles ocupando más sitios dentro del núcleo cristalino formado se inhibe la transferencia de masa de los TAG de mayor punto de fusión hacia el mismo.
También se observó que el efecto de los fitoesteroles sobre la cinética tuvo mayor influencia a bajos ∆TS. Si se compara la variación porcentual de disminución de la constante cinética a 38 y 40 ℃ de la mezcla sin agregado de fitoesteroles con respecto a la mezcla con un 4 % de fitoesteroles, fue de 27 y 92 %, respectivamente. Este tipo de comportamiento se ha observado para componentes menores o aditivos en materiales grasos (Cheong et al., 2009). El bloqueo de los fitoesteroles depende mayormente de que se adsorban en el núcleo cristalino, promoviendo un enlentecimiento del crecimiento cristalino. A un bajo ∆TS, se les brinda a las moléculas un tiempo adecuado para que puedan adoptar un empaquetamiento eficiente, siendo más probable que los fitoesteroles se adsorban y de esta forma actúen como un “bloqueador” para el crecimiento cristalino. En cambio, a altos ∆TS, la cristalización de los TAG es más favorable y los fitoesteroles tienen menos oportunidad de adsorberse en el núcleo cristalino.
Con respecto a los valores del exponente n, la adición de los fitoesteroles no modificó en forma apreciable la morfología cristalina, presentando en general un rango entre 1-2. Esto indica la presencia de morfología de tipo aguja y platos con una nucleación que varía entre esporádica e instantánea.
En la mezcla con 20 % de FHRBO y agregado de fitoesteroles a una Tc = 38 ℃, los fitoesteroles generaron un aumento de ti (como ocurrió con la otra mezcla); mientras que la k aumentó. Lo anterior indica que el efecto de los fitoesteroles depende de la concentración de TAG presentes con alta tendencia a cristalizar (fundamentalmente TAG S3). A bajas concentraciones de S3, los fitoesteroles estarían actuando como inductores de la cristalización.
La concentración requerida para lograr un determinado efecto en la cinética de cristalización difiere dependiendo del mecanismo por el cual actúa (Smith et al., 2011). Diferentes trabajos han reportado efectos similares de otros componentes menores (lecitinas, mono y diglicéridos) en la cinética de cristalización, influyendo en los ti, k y n obtenidos a partir del modelo de Avrami (Basso et al., 2010; Claro Silva et al., 2014; Miyasaki et al., 2016).
Conclusiones
Los resultados obtenidos mostraron que por medio de DSC es posible obtener información de interés en el estudio de la cinética de cristalización isotérmica en mezclas FHRBO/SBO con distintos contenidos de FHRBO y fitoesteroles a diferentes temperaturas de cristalización. El modelo de Avrami resultó útil y aplicable para la descripción de la cinética de cristalización en función de la cristalización relativa determinada a partir de la entalpia de cristalización.
Se observó que el aumento en la proporción de FHRBO en las mezclas produjo una gradual disminución del período de inducción (ti) y un aumento de la velocidad de crecimiento cristalino (k). La concentración de FHRBO es determinante sobre la velocidad de formación de núcleos cristalinos y su crecimiento posterior, lo que se atribuye al alto aporte de TAG del tipo S3 de alto punto de fusión. El grado de sobreenfriamiento (∆TS) también es un factor determinante sobre la cinética de la cristalización de las mezclas: a mayor grado, la cinética fue más rápida (menor ti y mayor k al comparar la misma mezcla a diferentes temperaturas de cristalización). Esto confirma la importancia del ∆TS sobre la tendencia a la cristalización de los materiales grasos.
El exponente de Avrami (n) no presentó, en ninguno de los casos, números enteros y se observaron en todas las mezclas y temperaturas de cristalización analizadas cambios en dicho parámetro. Esto sugiere cambios en la morfología y tipo de nucleación.
Dependiendo del mecanismo involucrado, la concentración de fitoesteroles puede influir en la cinética de cristalización. Ya sea por medio de la nucleación (ocupando sitios en el núcleo cristalino), el crecimiento (limitando la transferencia de masa de los TAG hacia el núcleo) o una combinación de ambas, se evidenciaron cambios en todas las concentraciones estudiadas. Se observó un aumento de ti y reducción de k, por lo que los fitoesteroles contribuyen a promover una cinética de cristalización más lenta, presentando un mayor efecto cuanto mayor es la concentración. El ∆TS influencia fuertemente el efecto de los fitoesteroles, especialmente al analizar la k a diferentes concentraciones. Cuanto mayor es el ∆TS, el efecto de los fitoesteroles se reduce.
Finalmente se determinó que, dependiendo de la mezcla estudiada, los fitoesteroles muestran un comportamiento diferente. La mezcla con 20 % de FHRBO provocó un incremento de ti y de k a medida que aumentó la concentración de fitoesteroles. En términos generales se observó que la concentración de FHRBO y de fitoesteroles en las mezclas afectaron los parámetros cinéticos obtenidos por el modelo de Avrami a partir de la cristalización isotérmica determinada por DSC. Por lo tanto, si bien los resultados obtenidos deben considerarse primarios y aplicados sobre determinadas condiciones, resulta un importante punto de partida para continuar investigando. Esto último es relevante en lo que se refiere al agregado de fitoesteroles, ya que se observaron cambios en el comportamiento de la cinética de cristalización. Los estudios realizados sugieren analizar con mayor profundidad el aporte de los fitoesteroles como ingrediente funcional y su influencia sobre la cinética de la cristalización que afectan las propiedades tecno-funcionales (textura y reología) de mezclas de materiales grasos y sus posibles aplicaciones. Lo mencionado anteriormente será de sumo interés para la industria alimentaria ya que permitirá tener un mejor diseño y control de las fases grasas comestibles.
Agradecimientos
Los autores agradecen al Programa de Apoyo a la Investigación Estudiantil (PAIE), perteneciente a la Comisión Sectorial de Investigación Científica (CSIC), por el financiamiento otorgado.
Referencias
Ali, M. A.; Islam M. A.; Othman, N. H.; Noor, A. M. e Ibrahim, M., 2019. Effect of rice bran oil addition on the oxidative degradation and fatty acid composition of soybean oil during heating. En: Acta Sci. Pol. Technol. Aliment., 18(4), pp. 427-438. DOI: https://doi.org/10.17306/J.AFS.2019.0694
American Oil Chemist´s Society, 2009a. Official methods and recommended practices of the American Oil Chemist´s Society (AOCS). 4th ed. Champaign: AOCS. Official Method Ch 3-91.
American Oil Chemist´s Society, 2009b. Official methods and recommended practices of the American Oil Chemist´s Society (AOCS). 4th ed. Champaign: AOCS. Official Method Ce 2-66
American Oil Chemist´s Society, 2009c. Official methods and recommended practices of the American Oil Chemist´s Society (AOCS). 4th ed. Champaign: AOCS. Official Method Ce 5b-89
American Oil Chemist´s Society, 2009d. Official methods and recommended practices of the American Oil Chemist´s Society (AOCS). 4th ed. Champaign: AOCS. Official Method Cj 1-94
Avrami, M., 1941. Kinetics of phase change III. Granulation, phase change, and microstructure. En: J. Chem. Phys., 9, pp. 177–184. DOI: https://doi.org/10.1063/1.1750872
Basso, R.; Badan Ribeiro, A. P.; Masuchi, M. H.; Gioielli, L. A.; Guaraldo Gonçalves, L.A.; Oliveira dos Santos, A.; Pavie Cardoso, L. y Grimaldi, R., 2010. Tripalmitin and monoacylglycerols as modifiers in the crystallization of palm oil. En: Food Chemistry, 122, pp. 1185–1192. DOI: https://doi.org/10.1016/j.foodchem.2010.03.113
Belitz, H. D.; Grosch, W. y Schieberle, P., 2009. Lipids. En: Belitz, H. D., Grosch, W. y Schieberle P. Food chemistry. 4th ed. Berlín: Springer. pp. 158-247.
Buscato, M. H.; Gallani, B.; Ramponi, K.; Badan Ribeiro, A. P. y Guenter, T., 2018. Modification of palm oil crystallization by phytosterol addition as a tool for structuring a low saturated lipid blend. En: Braz. J. Chem. Eng., 35(1), pp. 169-180. DOI: https://doi.org/10.1590/0104-6632.20180351s20160351
Callejas, N.; Suescun, L.; Badan, A. P. y Jachmanián, I., 2021. Zero-trans fats designed by enzyme-catalyzed interesterification of rice bran oil and fully hydrogenated rice bran oil. En: OCL, 28, 46. DOI: https://doi.org/10.1051/ocl/2021036
Cheong, L.; Zhang, H.; Xu, Y. y Xu, X., 2009. Physical characterization of lard partial acylglycerols and their effects on melting and crystallization properties of blends with rapeseed oil. En: J. Agric. Food Chem., 57(11), pp. 5020–5027. DOI: https://doi.org/10.1021/jf900665h
Claro Silva, R.; Schafer de Martin Soares, F. A.; Mayumi Muruyama, J.; Roque Dagostinho, N.; Silva, Y. A.; Andrade Calligaris, G.; Badan Ribeiro, A. P.; Paive Cardoso, L. y Gioielli, L. A., 2014. Effect of diacylglycerol addition on crystallization properties of pure triacylglycerols. En: Food Research International, 55, pp. 436-444. DOI: https://doi.org/10.1016/j.foodres.2013.11.037
Daels, E.; Foubert, I. y Goderis, B., 2017. The effect of adding a commercial phytosterol ester mixture on the phase behavior of palm oil. En: Food Research International, 100, pp. 841-849. DOI: https://doi.org/10.1016/j.foodres.2017.08.015
Daels, E.; Goderis, B.; Matton, V. y Foubert, I., 2018. Isothermal crystallization kinetics of palm oil as influenced by addition of a commercial phytosterol ester mixture. En: J. Agric. Food Chem., 66(15), pp. 3910–3921. DOI: https://doi.org/10.1021/acs.jafc.7b05049
Di Rienzo, J. A.; Casanoves, F.; Balzarini, M. G.; González, L.; Tablada, M. y Robledo, C. W. 2020. InfoStat [En línea]. Versión 29-09-2020. Córdoba: Universidad Nacional de Córdoba. [Consulta: 2 de Febrero de 2021]. Disponible en: http://www.infostat.com.ar.
Foubert, I.; Dewettinck, K. y Vanrolleghem, P. A., 2003. Modelling of the crystallization kinetics of fats. En: Trends in Food Science & Technology, 14(3), pp. 79-92. DOI: https://doi.org/10.1016/S0924-2244(02)00256-X
Gunstone, F. D. y Harwood, J. L., 2007. Occurrence and characterization of oils and fats. En: Gunstone, F. D., Harwood, J. L. y Dijkstra, A. J. The lipid handbook. 3a ed. New York: CRC Press. pp. 37-141.
Himawan, C.; Starov, V. M. y Stapley, A. G. F., 2006. Thermodynamic and kinetic aspects of fat crystallization. En: Adv Colloid Interface, 122, pp. 3–33. DOI: https://doi.org/10.1016/j.cis.2006.06.016
Hubbes, S. S.; Danzl, W. y Foerst, P., 2018. Crystallization kinetics of palm oil of different geographic origins and blends thereof by the application of the Avrami model. En: LWT, 93, pp. 189-196. DOI: https://doi.org/10.3390/foods11121769
Katan, M. B.; Grundy, S. M.; Jones, P.; Law, M.; Miettinen, T. y Paoletti, R., 2003. Efficacy and safety of plant stanols and sterols in the management of blood cholesterol levels. En: Mayo Clinic Proceeding, 78(8), pp. 965–978. DOI: https://doi.org/10.4065/78.8.965
Kawamura, K., 1980. The DSC thermal analysis of crystallization behavior in palm oil II. En: JAOCS, 57, pp. 48–52. DOI: https://doi.org/10.1007/BF02675525
Lu, C.; Qiu, S.; Wang, X.; He, X.; Dang, L. y Wang, Z., 2021. Contrastive analysis of lipid composition and thermal and crystallization behavior of olein/stearin fractionated by novel layer melt crystallization from palm oil. En: Journal of the Science of Food and Agriculture, 101(10), pp. 4350-4360. DOI: https://doi.org/10.1002/jsfa.11075
MacNaughtan, W.; Farhata, I. A.; Himawanb, C.; Starovb, V. M. y Stapley, A. G. F., 2006. A differential scanning calorimetry study of the crystallization kinetics of Tristearin-Tripalmitin mixtures. En: JAOCS, 83, pp. 1-9. DOI: https://doi.org/10.1007/S11746-006-1167-1
Marangoni, A. G., Introduction. 2013a. En: Marangoni, A. G. Structure and Properties of fat crystal networks. 2nd ed. Boca Raton: CRC Press. pp. xv-xviii.
Marangoni, A. G., Nucleation and Crystalline Growth Kinetics. 2013b. En: Marangoni A. G. Structure and Properties of fat crystal networks. 2nd ed. Boca Raton: CRC Press. pp. 27-96.
Marangoni, A. G., 2013c. Crystallography and polymorphism. En: Marangoni A. G. Structure and properties of fat crystal networks. 2a ed. Boca Raton: CRC Press. pp. 1-24.
Marangoni de Oliveira, G.; Ribeiro, A. P. B.; Oliveira dos Santos, A.; Cardoso, L. P. y Kieckbusch, T. G., 2015. Hard fats as additives in palm oil and its relationships to crystallization process and polymorphism. En: LWT, 63, pp. 1163–1170.
Marangoni, A. G., 2005. Crystallization kinetics. En: Marangoni, A. G. Fat crystal networks. 1a ed. New York: Marcel Dekker. pp. 21-83.
Metin, S. y Hartel, R. W., 2005. Crystallization of fats and oils. En: Shahidi, F. Bailey´s industrial oil and fat products. 6a ed. New Jersey: John Wiley & Sons. pp. 45-76.
Miyasaki, E. K.; Luccas, V. y Kieckbusch, T.G., 2016. Modified soybean lecithins as inducers of the acceleration of cocoa butter crystallization. En: Eur. J. Lipid Sci. Technol., 118, pp. 1539-1549. DOI: https://doi.org/10.1002/ejlt.201500093
Mursalin, M.; Hariyadi, P.; Purnomo, E. H.; Andarwulan, N. y Fardiaz, D., 2016. Crystallization kinetics of coconut oil based on Avrami model. En: International Food Research Journal, 23(4), pp. 1355-1360.
Narine, S. S.; Humphrey, K.L. y Laziz, B., 2006. Modification of the Avrami model for application to the kinetics of the melt crystallization of lipids. En: JAOCS, 83(11), pp. 913–921. DOI: https://doi.org/10.1007/s11746-006-5046-6
Ornla-ied, P.; Podchong, P. y Sonwai, S., 2021. Synthesis of cocoa butter alternatives from palm kernel stearin, coconut oil and fully hydrogenated palm stearin blends by chemical interesterification. En: Journal of the Science of Food and Agriculture, 102(4), pp. 1619-1627. DOI: https://doi.org/10.1002/jsfa.11498
Oteng, A. B. y Kersten, S., 2020. Mechanisms of action of trans fatty acids. En: Adv Nutr, 11(3), pp. 697–708. DOI: https://doi.org/10.1093/advances/nmz125
Ribeiro, A. P.; Grimaldi, R.; Gioielli, L. A. y Gonçalves, L., 2009. Zero trans fats from soybean oil and fully hydrogenated soybean oil: physico-chemical properties and food applications. En: Food Res Int., 42(3), pp. 401–410. DOI: https://doi.org/10.1016/j.foodres.2009.01.012
Sato, K., 2001. Crystallization behavior of fats and lipids: A review. En: Chemical Engineering Science, 56, pp. 2255-2265. DOI: https://doi.org/10.1016/S0009-2509(00)00458-9
Segura, N. y Jachmanián I., 2020. Zero-trans fats by enzymatic interesterification of blends beef tallow/rice bran oil. En: OCL, 27, 4. DOI: https://doi.org/10.1051/ocl/2019052
Sharples, A., 1966. Overall kinetics of crystallization. En: Sharples, A. Introduction to polymer crystallization. 1a ed. London: Edward Arnold Ltd. pp. 44-59
Shimadzu Corporation, 2009. Thermal analysis workstation TA-60WS [En línea]. Version 2.21. Kioto: Shimadzu Corporation. [Consulta: 4 de Noviembre de 2022]. Disponible en: https://shimadzu.com.au/ta-60ws
Smith, K. W.; Bhaggan K.; Talbot, G. y Van Malssen, K., 2011. Crystallization of fats: Influence of minor components and additives. En: JAOCS, 88, pp. 1085-1101. DOI: https://doi.org/10.1007/s11746-011-1819-7
Supaphol, P. y Spruiell, J. E., 2000. A New technique for using DSC melting endotherms to study isothermal bulk crystallization of semicrystalline polymers at low degrees of undercooling: Syndiotactic Polypropylene. En: Sci - Phys., 39, pp. 775–792. DOI: https://doi.org/10.1081/MB-100102487
Toro-Vazquez, J.; Dibildox-Alvarado, E.; Charo-Alonso, M.; Herrera-Coronado, V. y Gomez-Aldapa, C., 2002. The Avrami Index and the Fractal Dimension in Vegetable Oil Crystallization. En: JAOCS, 79(9), pp. 855–866. DOI: https://doi.org/10.1007/s11746-002-0570-y
Zuher, M. A., Rashid, N. A., Omar, Z. y Ahmad, N., 2018. The influence of chemical interesterification on the physicochemical and microstructural properties of palm stearin, palm kernel oil, rice bran oil and their blends. En: Malays. Appl. Biol., 47(2), pp. 57–69.


